Atommodellens Historia
uppladdat: 2018-09-23
Endast fyra element fanns i världen, spekulerade filosoferna i antikens Grekland.
Enligt dem bestod de fyra elementen av eld, luft, vatten och jord och var självaste
uppbyggnaden av allt och alla.
Men den första början på den atommodellen vi känner till år 2018 började 400 f.kr, då
Filosofen Demokritos hade en teori om att allting var uppbyggt i ännu mindre
beståndsdelar som var odelbara. Demokritos teori blev dock ignorerad på grund av de
“fyra elementens” popularitet.

John Dalton kan sägas ha kommit upp med den första atommodellen, en
simpel modell som endast hade 1 beståndsdel. Då varken protonen,
elektronen eller neutronen hade blivit upptäckt vid det här laget fanns
det inte mycket mer att lägga till i modellen. Den hade samma regler som
Demokritos tidigare filosoferat om, t.ex att atomen var odelbar men den
hade inget tomrum i sig som Demokritos också filosoferat om, det
skulle komma i senare modeller. År 1903 blev det återigen felaktigt uppbackat att atomen var odelbar.

Den andra modellen av en atom renderades år 1904 av
fysikern J.J Thomson och blev kallad “Plumpudding modellen” pga dess liknelse till
efterrätten med samma namn. Modellen bestod av en slags "protonpudding” med
elektroner “instoppade”. Det fanns inget tomrum eller neutron, endast en positivt
laddad “pudding” med negativa "elektron-russin”

Han hade upptäckt elektronen år 1897 genom att utföra experiment med katodstrålar
och teorier som Ernest Rutherford år 1896 hade kommit upp med Thomsons support
och uppmuntran.
Elektronerna kom med i Plum-pudding modellen men blev givna namnet “Corpuscles”
som senare skulle ändras till ordet “elektrons/elektroner”. Han, likt andra fysiker, spekulerade att
elektroner var de enda byggstenarna av atomen, vilket senare blev motbevisat.
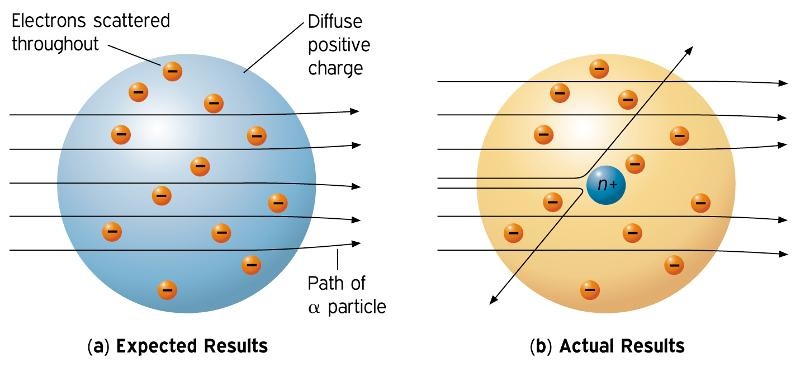
När Rutherford experimenterade senare, år 1911, tillsammans med sina elever.
Upptäckte han hur alfapartiklar som lyste igenom en tunn skiva gjord av guld inte bara
åkte rakt igenom materialet, utan under ett fåtal gånger också studsade åt andra håll.
Han uteslöt då att atomens protonska uppbyggnad verkligen var som en pudding och
kom fram till att dem flesta atomer har en protonsk kärna som inneslöts av elektroner
och en stor mängd tomrum, likt Demokritos andra teori om hur allt var uppbyggt av just
tomrum eller elementarpartiklar.
Det blev som en blandad version av Demokritos båda teorier och blev kallad
Kern-Hülle-modellen. 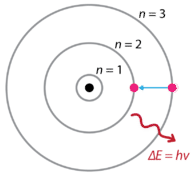
År 1913
förbättrade Niels Bohr, Rutherfords modell. Han studerade
väteatomens emissionsspektrum och kom fram till att elektroner endast
kunde finnas inom vissa bestämda banor och energinivåer. En elektron kunde också hoppa mellan dessa banor. Om den hoppade ned till en bana utsände den ljusstrålar samt om den hoppade upp till en yttre bana så infångades ljus.

Senare, år 1926
renderades den modellen vi använder idag med
matematiska ekvationer. Bohr utvecklade renderingen tillsammans med
fysikerna Werner Heisenberg och Erwin Schrödinger. Dem argumenterade
att det var omöjligt att förutse en bana och hastighet för en elektron och
att man istället skulle se elektronerna röra sig som i ett moln. Självaste
modellen blev då en så kallad “kvantmekanisk modell”
Rutherford hade också spekulerat sedan 20-talet att neutronen existerade inom
kärnan av atomen. Det var dock inte förrän under 1932 som James
Chadwick bevisade att neutronen fanns, tillsammans med protonen, som
en del av kärnan. Därför las även neutronen till i atom modellerna.
JÄMFÖRING AV MODELLER
:max_bytes(150000):strip_icc()/helium-atom-56a12c7d3df78cf7726820e5.jpg)
Den enklare atommodellen
Bohrs atommodell kan anses som en enklare version av den renderingen som kom efter.
Den är bättre att använda för atomer som har ett fåtal elektroner i sig än för tyngre
atomer. Den ger också felaktigt värde för marktillståndets orbitala vinkelmoment samt
bryter mot osäkerhetsprincipen då den visar att elektronerna som att dem åker i
bestämda banor med en satt radie (dessa 2 kan inte bestämmas samtidigt). Den är dock
enklare att tyda än den senaste orbitala modellen och är bättre för att visualisera hur en
atom fungerar.

Den orbitala modellen
Den orbitala modellen visar lite mer exakt än de andra modellerna. Den visar självklart
inte hur kärnan är utsmetad i tid och rum men är en mer exakt, men också mer
svåruppfattad. Den visar hur elektronerna åker runt som i moln, fortfarande med
bestämda banor men ej i skal med en satt radius. Modellen är baserad mer på Schrödingers matematiska ekvation för sannolikheten att hitta en elektron vid en viss
plats än en definierad bana.
Sluts
...läs fortsättningen genom att logga in dig.
Medlemskap krävs
För att komma åt allt innehåll på Mimers Brunn måste du vara medlem och inloggad.Kontot skapar du endast via facebook.
Källor för arbetet
NE.se [https://www.ne.se/uppslagsverk/encyklopedi/l%C3%A5ng/ernest-rutherford] Educational video [https://www.youtube.com/watch?v=DIC9uE_p2e4] Sutori.com [https://www.sutori.com/story/atommodellens-historia-eb55] Nobelprisets sida [https://www.nobelprize.org/prizes/chemistry/1908/rutherford/biographical/] FOF.se [https://fof.se/tidning/2003/7/artikel/john-dalton-atomen] ABCTE.org [http://www.abcte.org/files/previews/chemistry/s1_p6.html]
Kommentarer på arbetet
Inga kommentarer än :(
Liknande arbeten
-
 Inactive member
Inactive member
Källhänvisning
Jennifer Sandström [2018-09-23] Atommodellens HistoriaMimers Brunn [Online]. https://mimersbrunn.se/article?id=60418 [2024-04-25]

